»
Contoh soal hukum gas ideal
Contoh soal hukum gas ideal
1. Gas ideal berada di dalam suatu
ruang pada mulanya mempunyai volume V dan suhu T. Jika gas dipanaskan
sehingga suhunya berubah menjadi 5/4 T dan tekanan berubah menjadi 2P
maka volume gas berubah menjadi…
Pembahasan
Diketahui :
Volume awal (V
1) = V
Suhu awal (T
1) = T
Suhu akhir (T
2) = 5/4 T
Tekanan awal (P
1) = P
Tekanan akhir (P
2) = 2P
Ditanya : Volume akhir (V
2)
Jawab :
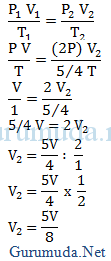
Volume gas berubah menjadi 5/8 kali volume awal.
2. Volume 2 mol gas pada suhu dan tekanan standar (STP) adalah…
Pembahasan
Diketahui :
Jumlah mol gas (n) = 2 mol
Suhu standar (T) = 0
oC = 0 + 273 = 273 Kelvin
Tekanan standar (P) = 1 atm = 1,013 x 10
5 Pascal
Konstanta gas umum (R) = 8,315 Joule/mol.Kelvin
Ditanya : Volume gas (V)
Jawab :
Hukum Gas Ideal (dalam jumlah mol, n)

Volume 2 mol gas adalah 44,8 liter.
Volume 1 mol gas adalah 45,4 liter / 2 = 22,4 liter.
Jadi volume 1 mol gas, baik gas oksigen atau helium atau argon atau gas lainnya, adalah 22,4 liter.
3. 4 liter gas oksigen bersuhu 27°C pada tekanan 2 atm (1 atm = 10
5 Pa) berada dalam sebuah wadah. Jika konstanta gas umum R = 8,314 J.mol
−1.K
−1 dan bilangan avogadro N
A 6,02 x 10
23 molekul, maka banyaknya molekul gas oksigen dalam wadah adalah…
Pembahasan
Diketahui :
Volume gas (V) = 4 liter = 4 dm
3 = 4 x 10
-3 m
3
Suhu gas (T) = 27
oC = 27 + 273 = 300 Kelvin
Tekanan gas (P) = 2 atm = 2 x 10
5 Pascal
Konstanta gas umum (R) = 8,314 J.mol
−1.K
−1
Bilangan Avogadro (N
A) = 6,02 x 10
23
Ditanya : Banyaknya molekul gas oksigen dalam wadah (N)
Jawab :
Konstanta Boltzmann :
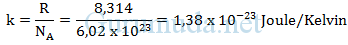 Hukum Gas Ideal (dalam jumlah molekul, N)
Hukum Gas Ideal (dalam jumlah molekul, N)

Dalam 1 mol gas oksigen, terdapat 1,93 x 10
23 molekul oksigen.
4. Sebuah bejana berisi gas neon (Ne, massa atom = 20 u) pada suhu dan tekanan standar (STP mempunyai volume 2 m
3. Tentukan massa gas neon!
Diketahui :
Massa atom neon = 20 gram/mol = 0,02 kg/mol
Suhu standar (T) = 0
oC = 273 Kelvin
Tekanan standar (P) = 1 atm = 1,013 x 10
5 Pascal
Volume (V) = 2 m
3
Ditanya : massa (m) gas neon
Jawab :
Pada suhu dan tekanan standar (STP), 1 mol gas apa saja, termasuk gas neon, mempunyai volume 22,4 liter = 22,4 dm
3 = 0,0448 m
3. Dengan demikian, dalam volume 2 m
3 terdapat berapa mol gas neon ?
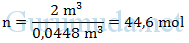
Dalam volume 2 m
3 terdapat 44,6 mol gas neon.
Massa atom relatif gas neon adalah 20 gram/mol. Ini artinya dalam 1 mol
terdapat 20 gram atau 0,02 kg gas neon. Karena dalam 1 mol terdapat 0,02
kg gas neon maka dalam 44,6 mol terdapat (44,6 mol)(0,02 kg/mol) =
0,892 kg = 892 gram gas neon.
Soal No. 1 16 gram gas Oksigen (M = 32 gr/mol) berada pada tekanan 1 atm dan suhu 27
oC. Tentukan volume gas jika:
a) diberikan nilai R = 8,314 J/mol.K
b) diberikan nilai R = 8314 J/kmol.K
Pembahasan a) untuk nilai R = 8,314 J/mol.K
Data :
R = 8,314 J/mol.K
T = 27
oC = 300 K
n = 16 gr : 32 gr/mol = 0,5 mol
P = 1 atm = 10
5 N/m
2 
b) untuk nilai R = 8314 J/kmol.K
Data :
R = 8314 J/kmol.K
T = 27
oC = 300 K
n = 16 gr : 32 gr/mol = 0,5 mol
P = 1 atm = 10
5 N/m
2  Soal No. 2
Soal No. 2 Gas bermassa 4 kg bersuhu 27
oC berada dalam tabung yang berlubang.

Jika tabung dipanasi hingga suhu 127
oC, dan pemuaian tabung diabaikan tentukan:
a) massa gas yang tersisa di tabung
b) massa gas yang keluar dari tabung
c) perbandingan massa gas yang keluar dari tabung dengan massa awal gas
d) perbandingan massa gas yang tersisa dalam tabung dengan massa awal gas
e) perbandingan massa gas yang keluar dari tabung dengan massa gas yang tersisa dalam tabung
Pembahasan Data :
Massa gas awal m
1 = 4 kg
Massa gas tersisa m
2 Massa gas yang keluar dari tabung Δ m = m
2 − m
1 a) massa gas yang tersisa di tabung

b) massa gas yang keluar dari tabung

c) perbandingan massa gas yang keluar dari tabung dengan massa awal gas

d) perbandingan massa gas yang tersisa dalam tabung dengan massa awal gas

e) perbandingan massa gas yang keluar dari tabung dengan massa gas yang tersisa dalam tabung
 Soal No. 3
Soal No. 3 A dan B dihubungkan dengan suatu pipa sempit. Suhu gas di A adalah 127
oC dan jumlah partikel gas di A tiga kali jumlah partikel di B.

Jika volume B seperempat volume A, tentukan suhu gas di B!
Pembahasan Data :
T
A = 127
oC = 400 K
N
A : N
B = 2 : 1
V
A : V
B = 4 : 1
 Soal No. 4
Soal No. 4 Gas dalam ruang tertutup memiliki suhu sebesar T Kelvin energi kinetik rata-rata Ek = 1200 joule dan laju efektif V = 20 m/s.

Jika suhu gas dinaikkan hingga menjadi 2T tentukan:
a) perbandingan energi kinetik rata-rata gas kondisi akhir terhadap kondisi awalnya
b) energi kinetik rata-rata akhir
c) perbandingan laju efektif gas kondisi akhir terhadap kondisi awalnya
d) laju efektif akhir
Pembahasan a) perbandingan energi kinetik rata-rata gas kondisi akhir terhadap kondisi awalnya

b) energi kinetik rata-rata akhir

c) perbandingan laju efektif gas kondisi akhir terhadap kondisi awalnya

d) laju efektif akhir
 Soal No. 5
Soal No. 5
Sebuah ruang tertutup berisi gas ideal dengan suhu T dan kecepatan
partikel gas di dalamnya v. Jika suhu gas itu dinaikkan menjadi 2T maka
kecepatan partikel gas tersebut menjadi …
A. √2 v
B. 12 v
C. 2 v
D. 4 v
E. v
2
(Dari soal Ebtanas 1990)
Pembahasan Data dari soal adalah:
T
1 = T
T
2 = 2T
V
1 = ν
v
2 =.....
Kecepatan gas untuk dua suhu yang berbeda

Sehingga diperoleh
 Soal No. 6
Soal No. 6 Didalam sebuah ruangan tertutup terdapat gas dengan suhu 27
oC. Apabila gas dipanaskan sampai energi kinetiknya menjadi 5 kali energi semula, maka gas itu harus dipanaskan sampai suhu …
A. 100
oC
B. 135
oC
C. 1.200
oC
D. 1.227
oC
E. 1.500
oC
(Soal Ebtanas 1992)
Pembahasan Data diambil dari soal
T
1 = 27°C = 27 + 273 = 300 K
Ek
2 = 5 Ek1
T
2 = .....
Energi kinetik gas untuk dua suhu yang berbeda

Sehingga diperoleh

Dalam Celcius adalah = 1500 − 273 = 1227°C
Soal No. 7
Di dalam ruang tertutup suhu suatu gas 27°C, tekanan 1 atm dan volume
0,5 liter. Jika suhu gas dinaikkan menjadi 327°C dan tekanan menjadi 2
atm, maka volume gas menjadi....
A. 1 liter
B. 0,5 liter
C. 0,25 liter
D. 0,125 liter
E. 0,0625 liter
Pembahasan Data soal:
T
1 = 27°C = 300 K
P
1 = 1 atm
V
1 = 0,5 liter
T
2 = 327°C = 600 K
P
2 = 2 atm
V
2 = ..........
P
1 V
1 P
2 V
2 _______ = _______
T
1 T
2 (1)(0,5) (2) V
2 _______ = _______
300 600
V
2 = 0,5 liter
Soal No. 8
Suatu gas ideal mula-mula menempati ruang yang volumenya V dan tekanan
P. Jika suhu gas menjadi 5/4 T dan volumenya menjadi 3/4 V, maka
tekanannya menjadi….
A. 3/4 P
B. 4/3 P
C. 3/2 P
D. 5/3 P
E. 2 P
(UN 2010 PO4) Pembahasan  Soal No. 9
Soal No. 9
Gas dengan volume V berada di dalam ruang tertutup bertekanan P dan
bersuhu T. Bila gas mengembang secara isobarik sehingga volumenya
menjadi 1/2 kali volume mula-mula, maka perbandingan suhu gas mula-mula
dan akhir adalah....
(UN Fisika 2014) A. 1 : 1
B. 1 : 2
C. 1 : 3
D. 2 : 1
E. 3 : 2
Pembahasan Data soal:
P
1 = P → 1
T
1 = T → 1
Isobaris artinya tekanannya sama P
1 = P
2 → 1
Volumenya menjadi 1/2 kali volume mula-mula artinya:
V
2 = 1
V
1 = 2
T
1 : T
2 =....
 Soal No. 10
Soal No. 10 Suatu gas ideal mula-mula menempati ruangan yang volumenya V dan suhu T dan tekanan P.
Tabung I Tabung II 
Jika gas dipanaskan kondisinya seperti pada tabung 2, maka volume gas menjadi....
(UN Fisika 2014) A. 1/2 V
B. 8/9 V
C. 9/8 V
D. 2/3 V
E. 3/2 V
Pembahasan Data soal:
Tekanan menjadi 4/3 mula-mula:
P
1 = 3
P
2 = 4
Suhu menjadi 3/2 mula-mula:
T
1 = 2
T
2 = 3
V
2 = ..... V
1 